24 دی اهمیت سنجش وتشخیص HCP و روشهای مورداستفاده جهت سنجش آنها
تشخیص HCP یا تشخیص و حذف پروتئین های سلول میزبان در محصولات نوترکیب درمانی یک اقدام ضروری است. از طرفی فرایندهای تصفیه محصول باید به طور مرتب بهینهسازی شوند تا بتوان در حد امکان HCPها را حذف یا غیرفعال کرد.
سنجش HCP اطلاعات مهمی از جمله ترکیب مواد وارد شده به فرایند و تأثیر هر مرحله بر پاکسازی HCP ارائه میدهد؛ بنابراین بررسی خصوصیات فرایند و اعتبارسنجی آن امری ضروری است. بهاینترتیب، سنجش HCP بخش اساسی توسعه فرایند تصفیه است و به اطمینان از ثبات تولید کمک میکند. در نهایت، برای اندازهگیری HCPهای موجود در محصول دارویی نهایی به متدهای سنجش HCP تکرارپذیر و قابلاعتماد نیاز است.
ازآنجاییکه این HCPها به طور بالقوه ایمونوژن هستند، یکی از راههای مناسب برای ارزیابی حضور HCPها استفاده از روشهای مبتنی بر ایمنی سنجی است. رایجترین نوع آن روش ایمنی سنجی ساندویچ است که از سیستم تشخیصی مبتنی بر آنزیم (ELISA)، رنگسنجی، الکتروکمی لومینسانس (ECL) یا موارد دیگر استفاده میشود. این روش دارای حساسیت و اختصاصیت بالا بوده و از طرفی میتواند نتایج را بهصورت کمی ارائه دهد و از نظر اقتصادی مقرونبهصرفه است. سایر روشهای ایمنی سنجی (بهعنوانمثال، ایمنی سنجی رقابتی) نیز وجود دارند که حساسیت و اختصاصیت آنها پایینتر از روش ایمنی سنجی ساندویچ است.
در این روش از آنتیبادیهای پلیکلونال جهت شناسایی انواع HCPها استفاده میگردد. جهت تولید آنتیبادیهای ضد HCP، مخلوط HCP را به حیوانی مانند خرگوش، بز یا مرغ تزریق میکنند. پاسخ ایمنی ایجاد شده در حیوانات سبب تولید آنتیبادیهای ضد HCP میگردد. آنتیبادیهای پلیکلونال تولید شده در حیوانات باید قادر به تشخیص همه و یا اکثر پروتئینهای موجود در مخلوط HCP باشند.
علاوه بر روش ایمنی سنجی، انواع دیگر سنجشها مانند الکتروفورز، پروتئومیکس و کروماتوگرافی نیز وجود دارند که میتوانند بهعنوان تستهای تأییدی و مکمل پس از روش ایمنی سنجی مورداستفاده قرار گیرند.
در اینجا تشخیص HCP با استفاده از روشهای الکتروفورز، وسترنبلات و پروتئومیکس و مزایا و معایب هرکدام از آنها را ذکر میکنیم.
تشخیص HCP با استفاده از روش الکتروفورز
سه روش الکتروفورز برای آنالیز ناخالصی عبارتاند از: SDS-PAGE 1-D، SDS-PAGE 2-D و الکتروفورز موئینهای SDS با استفاده از صافی غیرژلی (CE-SDS). در تمام این روشها، مقداری از نمونه برای تشخیص ناخالصیهای پروتئینی بر روی ژل بارگذاری میشود. وجود یک نوار جدید در ژل، یا یک پیک جدید در الکتروفروگرام CE-SDS، میتواند نشاندهنده وجود یک ماده جدید یا ناخالصی مرتبط با محصول باشد و یا نشاندهنده ناخالصی HCP است. از الکتروفورز مبتنی بر ژل و الکتروفورز موئینهای SDS با صافی غیر ژلی ( CE-SDS) میتوان بهعنوان تست تأییدی برای اثبات وجود ناخالصی پس از تست ایمونواسی استفاده کرد. درصورتیکه برخی از HCPها در روش ایمنی سنجی شناسایی نشده باشند، با استفاده از این روش میتوان آنها را شناسایی کرد. ژلها معمولاً با رنگهایی با حساسیت بالا مانند فلوروفور یا نقره رنگ میشوند. در حالت ایدئال، رنگ باید با هضم پروتئولیتیک درون ژل و نیز آنالیزهای بعدی توسط طیفسنجی جرمی برای شناسایی پروتئین سازگار باشد. یکی از معایب این روش این است که ممکن است ناخالصیها به باند محصول بسیار نزدیک شوند. در این صورت تداخل ایجاد شده و ناخالصیها شناسایی نمیشوند.
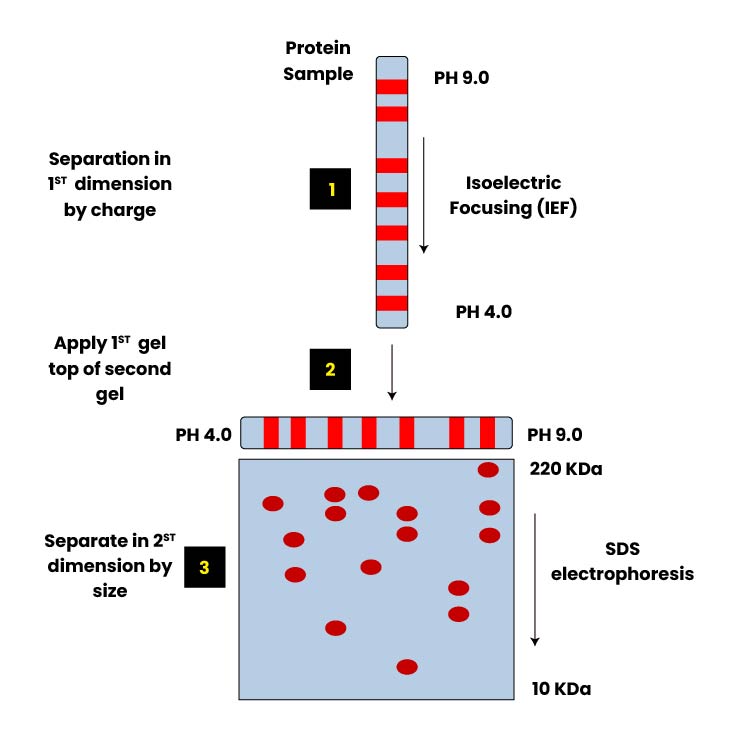 روش الکتروفورز SDS-PAGE 1-D و SDS-PAGE 2-D
روش الکتروفورز SDS-PAGE 1-D و SDS-PAGE 2-D
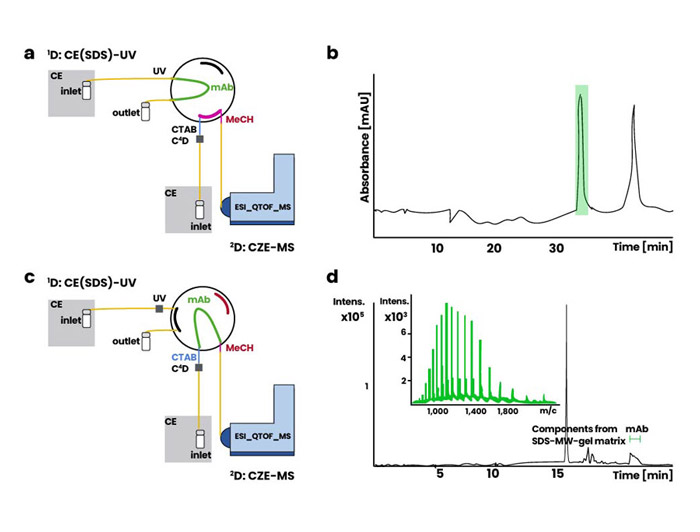 الکتروفورز موئینهای SDS با صافی غیر ژلی (CE-SDS)
الکتروفورز موئینهای SDS با صافی غیر ژلی (CE-SDS)
جدول 1. ویژگیها، مزایا و معایب روش الکتروفورز برای تشخیص HCP
|
روش |
موارد استفاده |
مزایا |
معایب |
حساسیت تقریبی برای HCPها و توانایی کمیسازی |
|
ژل یکبعدی (1-D)، احیا شده یا غیر احیا شده، رنگآمیزی شده با رنگ نقره یا رنگ فلورسنت با حساسیت بالا |
· غربالگری تعداد زیادی نمونه از نظر قوام و وجود لکههای پروتئینی ناشناخته · تعیین باندهای پروتئینی غیراختصاصی · استفاده بهعنوان بخشی از سیستم کنترل GMP |
· جداسازی ناخالصیهای HCP از محصول با وضوح بالا · ساده و آسان بودن تست · تعیین وزن مولکولی تقریبی · تجزیهوتحلیل جانبی نمونهها که امکان مقایسه برای ثبات تولید را فراهم میکند. |
· وجود مقدار زیاد پروتئین محصول که ممکن است باندهای HCP را پنهان کند. · بهصورت نیمه کمی است و تنها تفاوت پروتئینها را بر اساس شدت رنگ نشان میدهد. · دارای ظرفیت محدودی در خطوط ژل برای بار کل پروتئین است. |
ng/mg 100 نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. |
|
ژل دوبعدی (2-D) با فرمت بزرگ (بهعنوانمثال،20 × 25 سانتیمتر) رنگآمیزی شده با رنگ نقره یا یک رنگ فلورسنت با حساسیت بالا |
· غربالگری تعداد کمی از نمونهها از نظر قوام و وجود لکههای پروتئینی ناشناخته
· برای استفاده معمول رایج نیست؛ اما ممکن است برای توصیف برخی از Lotها و یا استاندارد HCP مورداستفاده قرار گیرد. |
· جداسازی ناخالصیهای HCP از محصول با وضوح بالا
· تعیین وزن مولکولی (MW) تقریبی و PI از لکههای پروتئینی ایجاد شده |
· وجود مقدار زیاد پروتئین محصول ممکن است لکههای HCP را پنهان کند.
· بهصورت نیمه کمی است و تنها تفاوت پروتئینها را بر اساس شدت رنگ نشان میدهد. · نیاز به تجهیزات پیچیده دارد. · باید توسط یک تکنسین ماهر و مجرب انجام گیرد. |
ng/mg 100 (از پروتئین کل)
نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. |
|
CE-SDS مبتنی بر فلورسانس القا شده توسط لیزر (LIF) نمونههای نشاندار شده با فلورسنت بهعنوان نمونههای احیا شده یا غیر احیا شده جدا میشوند. |
· غربالگری تعداد زیادی نمونه از نظر قوام و وجود پیکهای پروتئینی ناشناخته
· امکان استفاده بهعنوان بخشی از سیستم کنترل GMP |
· روشی سریع و با وضوح بالا برای جداسازی پروتئینهای نشاندار شده با فلورسنت | · حساسیت کمتر نسبت به روش ژل یکبعدی
· نشانگرهای فلورسنت برای HCPها اختصاصی نیستند، بنابراین هیچ تمایزی بین HCP و پپتیدهای مرتبط با محصول وجود ندارد. · شناسایی پیکهای پروتئین دشوار است. |
ng/mg 1000 (1/0 درصد از کل بار پروتئین)
نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. |
تشخیص HCP با استفاده از روش وسترن بلات
تکنیک وسترن به لات بهعنوان روش مکمل ایمنی سنجی ساندویچ جهت نشاندادن خلوص محصول و نیز مشخصکردن معرفهای ایمونوشیمیایی مورداستفاده قرار میگیرد. در این روش از آنتیبادی ضد HCP بهعنوان یک پروب استفاده میشود. با این روش میتوان HCPهای معین را شناسایی کرد. همچنین از این روش میتوان برای شناسایی HCPهایی که به طور غیرکوالانسی به محصول متصل شدهاند و در سنجش ایمنی شناسایی نشدهاند استفاده کرد؛ بنابراین روش بلات میتواند اطلاعات بیشتری را در مورد پروتئینهای کمیاب و یا شناسایی نشده ارائه دهد. البته ممکن است پروتئینی که در روش ایمنی سنجی بهخوبی واکنش نشان داده، در وسترن بلات شناسایی نشود. زیرا ممکن است به دنبال دناتورهشدن پروتئین، یکی از اپیتوپهای ساختاری آن از بین رفته باشد. یکی دیگر از مزایای این روش این است که ایمونوبلات فقط به یک آنتیبادی برای پروتئین معین نیاز دارد، درحالیکه ایمنی سنجی ساندویچ به دو آنتیبادی نیاز دارد. همچنین این روش به دلیل استفاده از آنتیبادیهای با میل ترکیبی بالا برای واکنش با HCP معین، حساستر از رنگآمیزی نقره یا رنگ فلورسنت ژلها است.
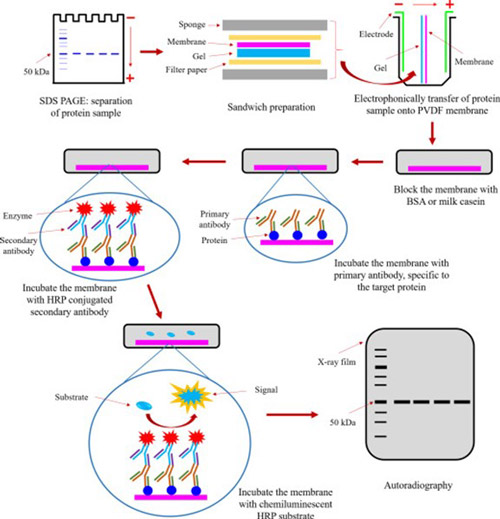
تشخیص HCP با استفاده از روش وسترن بلات
جدول 2. ویژگیها، مزایا و معایب روش وسترن بلات برای تشخیص HCP
|
روش |
موارد استفاده |
مزایا |
معایب |
حساسیت تقریبی و توانایی کمیسازی HCP |
|
ژل یکبعدی (1-D)، وسترن بلات |
· غربالگری تعداد زیادی نمونه از نظر قوام و وجود باندهای پروتئینی ناشناخته که با آنتیبادیهای ضد HCP واکنش میدهند. · امکان استفاده بهعنوان بخشی از سیستم کنترل GMP |
· جداسازی ناخالصیهای HCP از محصول با وضوح بالا · تعیین اطلاعات تقریبی از وزن مولکولی · سادگی و آسان بودن تست · تجزیهوتحلیل جانبی نمونهها که امکان مقایسه برای ثبات تولید را فراهم میکند. |
· نیاز به آنتیبادی ضد HCP باکیفیت بالا · وجود مقادیر زیاد محصول که منجر به ایجاد باندهای غیراختصاصی میگردد. · دناتورهشدن پروتئینهای ناشی از SDS که منجر به ازدستدادن اپیتوپهای ساختاری میشود. |
نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. حساسیت کاملاً به کیفیت آنتیبادی بستگی دارد. |
|
ژل دوبعدی (2-D) با فرمت بزرگ (بهعنوانمثال، 20 × 25 سانتیمتر) وسترن بلات بر مبنای کمی لومینسانس یا هرگونه تشخیص مشابه با حساسیت بالا |
· غربالگری تعداد کمی از نمونهها از نظر قوام و وجود لکههای پروتئینی ناشناخته در واکنش با آنتیبادیهای HCP · برای استفاده معمولی مناسب نیست، اما ممکن است برای مشخصکردن تعداد زیادی از محصولات خاص یا مشخصکردن معرفهای آنتیبادی استفاده شود. |
· جداسازی ناخالصیهای HCP از محصول با وضوح بالا · تعیین میزان تقریبی وزن مولکولی (MW) و PI از نقاط پروتئینی ایجاد شده |
· نیاز به آنتیبادی ضد HCP باکیفیت بالا · وجود مقادیر زیاد محصول منجر به پنهانشدن لکههای HCP میشود. · دناتورهشدن پروتئینهای ناشی از SDS منجر به ازدستدادن اپیتوپهای ساختاری میشود. · نیاز به تکنسین مجرب و ماهر دارد. |
ng/mg 100 نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. حساسیت کاملاً به کیفیت آنتیبادی بستگی دارد. |
تشخیص HCP با استفاده از روش پروتئومیکس و کروماتوگرافی
تکنیکهای طیفسنجی جرمی برای تشخیص، شناسایی و تعیین کمی HCPها بهسرعت در حال تکامل هستند و اغلب از فناوریهای توسعهیافته برای پروتئومیکس استفاده میکنند. با در دسترس قرارگرفتن پایگاههای داده ژنومی جدید (بهعنوانمثال، ژنوم CHO)، روشهای طیفسنجی جرمی مفیدتر هستند. یکی از مزایای این روش توانایی شناسایی آنالیتهای متعدد در یک نمونه با سرعت بالا است. علاوه بر این، با این روش میتوان مقادیر بسیار کم HCPها را تشخیص داد. این امر بسیار حائز اهمیت است؛ زیرا مقادیر بسیار کم این ناخالصیها میتوانند بر فراورده دارویی تأثیر منفی گذاشته و سبب تحریک ایمنیزایی گردد. در این روش ابتدا نمونه را تحت فرایندهایی مانند احیا، آلکیلاسیون و هضم پروتئولیتیک قرار میدهند. به دنبال آن جداسازی (بهعنوانمثال با کروماتوگرافی فاز معکوس RP-HPLC) را قبل از معرفی به یک طیفسنج جرمی انجام میدهند. تمامی پروتئینها تجزیه میشوند، بنابراین یک توالی اسیدآمینه برای هر پپتید فراهم میکند. اطلاعات توالی حاصل با توالی محصول برای شناسایی قطعات مرتبط با محصول و با پایگاهداده مربوط به میزبان (بهعنوانمثال، E. Coli، CHO) برای شناسایی HCP مقایسه میشود. یکی از چالشهای طیفسنجی جرمی (MS) تعداد زیاد پپتیدهای مشتق شده از محصول نسبت به پپتیدهای ناخالصی است.
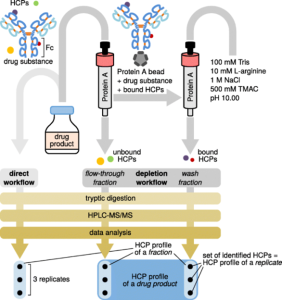 تشخیص HCP با استفاده از روش کروماتوگرافی
تشخیص HCP با استفاده از روش کروماتوگرافی
جدول 3. ویژگیها، مزایا و معایب روش کروماتوگرافی برای تشخیص HCP
|
روش |
موارد استفاده |
مزایا |
معایب |
|
|
اسپکترومتری جرمی یونیزاسیون الکترو اسپری (ESI)/HPLC cIEF/ESI-MS/MS MALDI-TOF |
· شناسایی HCPهای شخصی · توصیف یک محصول خالص شده یا استانداردهای HCP سلول نول (null) |
· امکان شناسایی و نظارت بر HCPهای فردی را فراهم میکند. · ممکن است با ژلها ترکیب شود تا تکتک پروتئینهای موجود در ژلها را شناسایی کند. |
· نیاز به تکنسین ماهر و مجرب دارد. · نیاز به ابزار دقیق و پیچیده دارد.
|
· برای جستجوی HCPهای ناشناخته نیمه کمی است (ng/mg100). · درصورتیکه با یک استاندارد تحلیلی برای HCPهای شناخته شده استفاده گردد بهصورت کمی است (ng/mg10). |
|
RP-HPLC/UV RPUHPLC/UV |
· اگر پروتئینها بهخوبی از هم جدا شده باشند، برای مقایسه استانداردهای اجزای سلول نول (null) مناسب است. · پروتئینهای بزرگتر ممکن است برای بهبود وضوح به پروتئولیز یا احیا به میزان محدود نیاز داشته باشند. |
· کیفیت بالا
· جداسازی HCPها بر اساس آبگریزی و اندازه
|
· پیداکردن یک فاز ثابت و فاز متحرک که بتواند تمام HCPها را حل کرده و شستشو دهد مشکل است. · شستشو ممکن است برخی از پروتئینهای خاص را مختل کند. · غلظت بالای پروتئین محصول ممکن است در تشخیص HCP اختلال ایجاد کند. |
ng/mg10000 نیمه کمی است، مگر اینکه با یک استاندارد تحلیلی برای یک HCP شناخته شده استفاده شود. |




No Comments